アミロイドMSとは
「アミロイドMS」とは、島津製作所と国立研究開発法人国立長寿医療研究センター(以下、長寿研)が開発した、アルツハイマー病をスクリーニングするための新しい血液分析法です。血液数滴(約0.5 mL)から、早期のアルツハイマー病の予測を目指す技術です。
アルツハイマー病について
近年、高齢化の進展とともに、認知症の患者数も増加しています。平成24年度の時点では65歳以上の高齢者における7人に1人が認知症であり、今後も増え続けると予想されています。厚生労働省と関係省庁が認知症施策推進総合戦略(新オレンジプラン)を立ち上げるなど、認知症対策は社会課題となっており、早期発見法・治療法・予防法の確立が求められています。認知症の原因となる主な疾患は様々(アルツハイマー型認知症、脳血管性認知症、レビー小体型認知症、前頭側頭型認知症など)ですが、中でもアルツハイマー型認知症が最も多く患者数は全体の約6割を占めています。
アルツハイマー型認知症の原因は未だ解明されていませんが、進行に伴っていくつかの特有の病変が見られることがわかっています。例えば、神経細胞の外側では「アミロイドβ」が蓄積して老人班を形成し、神経細胞の中では「タウタンパク」が蓄積してタンパク質が糸くず状に変化したようなもの(神経原繊維変化)が見られるようになります。
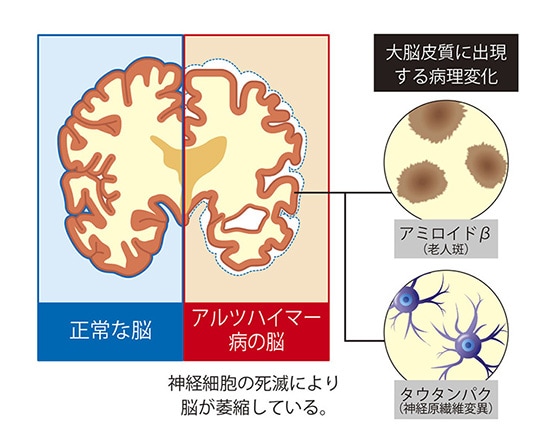
そこで、「認知機能の低下」という症状が出る前にアルツハイマー病変を捉える方法の1つとして、「アミロイドβ」や「タウタンパク」の蓄積状態(量、濃度、分布)を可視化、数値化するというものがあります。例えば、PET検査や脳脊髄液(CSF)マーカー検査です。
また、島津製作所と国立研究開発法人国立長寿医療研究センター(長寿研)が共同して、血液数滴からアミロイドβの蓄積量を推定するのに有効なバイオマーカーを発見しました。
アミロイドβ関連ペプチドを正確に検出するまで
たとえアミロイドβが蓄積している状態であっても、血中には様々な夾雑物(きょうざつぶつ・あるものの中に混じっている余計なものの意)が高濃度に存在し、アミロイドβはごく少量です。血液を採取しても、その中からアミロイドβを検出することは困難でした。
また、アミロイドβは、40個のアミノ酸が結合したペプチド“Aβ1-40”と42個のアミノ酸が結合したペプチド“Aβ1-42”の2種類が主に知られていますが、それ以外の長さのものが10種類以上存在することがわかっていました。従来から知られる免疫測定法(ELISA)は、複数の長さのアミロイドβをまとめて測り取る性質の測定法であり、Aβ1-40とAβ1-42を見分けることはできても、その他のAβ関連ペプチド(様々な長さのアミロイドβの総称)を正確に測定することはできませんでした。
そこで、島津製作所は、質量分析が多種類の物質の同定および同時測定に強いことに着目し、2010年に参加した最先端研究開発支援プログラム(FIRST)の成果である高性能の質量分析システムを使ってアミロイドβ関連ペプチドを測定することを考えました。
ごく微量なアミロイドβ関連ペプチドを質量分析装置で検出することは技術的に困難でしたが、血液の前処理方法を確立することによりこの問題を打破しました。さらに、長寿研との共同研究により、アミロイドβの蓄積状態と相関のあるバイオマーカーを発見し、世界で初めて血液でのアミロイド蓄積の予測を可能する技術を開発しました。
-

血液採取

-

血液の前処理

-

質量分析

-

アミロイドβ関連ペプチドの分析
イノベーション1.血液の前処理方法
各アミロイドβ関連ペプチドの量をそれぞれ正確に検出するために、島津製作所の金子さんは様々な血液の前処理方法を試しました。
そして、アミロイドβ関連ペプチド内の配列に対するエピトープを持つ特殊な抗体を用いて、アフィニティ精製を2回連続で行う方法を見出しました。
抗原抗体反応に最適な界面活性剤を選択すること、第一工程では界面活性剤を、第二工程では有機溶媒を酸性溶液に含ませるといったように各工程で最適な試薬を使用すること、さらに抗体に接触させる溶液の液量を適切に調整することなどの工夫により、血液中のアミロイドβ関連ペプチドだけを取り出し質量分析装置によってS/N比が十分ある状態で検出できることを発見しました。
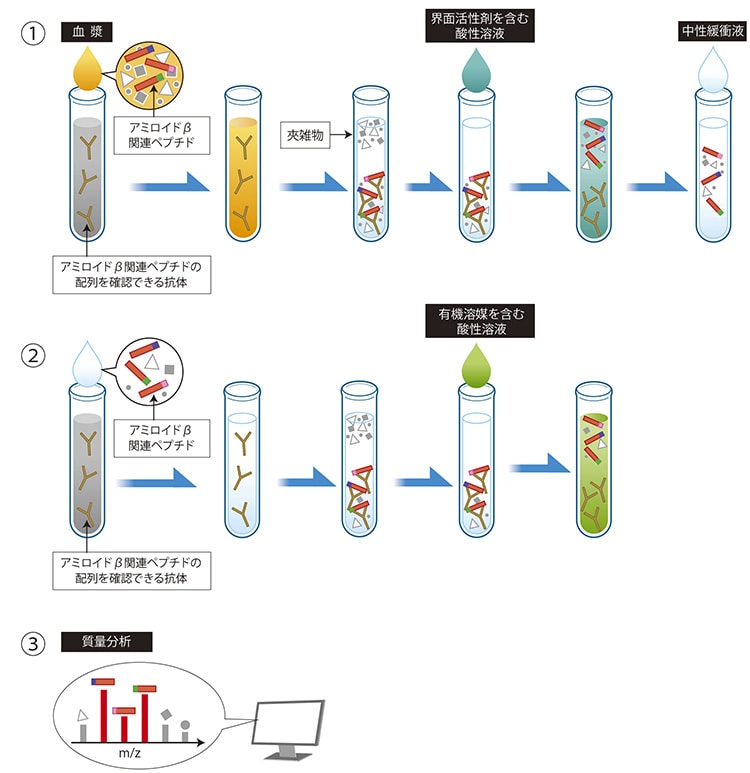
島津製作所の強みである“抗体技術”と“MALDIをイオン源とする(※)高性能な質量分析技術”を組み合わせる本手法により、22種類のアミロイドβ関連ペプチドを分離して、測定することができます。22種類には、今まで血液中での存在が確認されなかった新たな8種類のペプチドも含まれます。
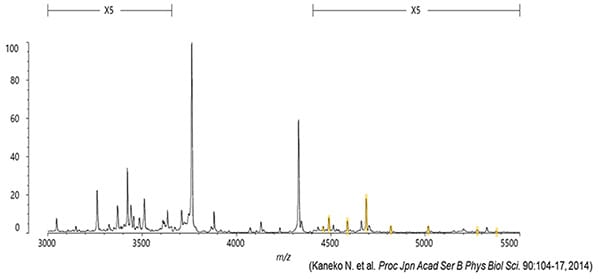
・ 特許番号:特許第06424757号
・ 論文:Proc. Jpn. Acad., Ser. B (2014) 90, 104-17
2.アミロイドβの蓄積状態の評価方法(バイオマーカー)
血液の前処理と高精度な質量分析システムにより、新規発見8種類を含め22種類のアミロイドβ関連ペプチドを測定することができます。では、「得られたデータは、アルツハイマー型認知症の早期発見にどう活用できるのか?」
知見を得るために、長寿研の門をたたきアルツハイマー病研究の第一人者である柳澤先生との共同研究が始まりました。
長寿研の柳澤先生は、臨床研究において明確な基準で陰性と陽性を分けるため、これまでに一般的に用いられていた「問診結果」ではなく「Aβ-PET検査結果」を基準にしてバイオマーカー探索を行うことを提案しました。
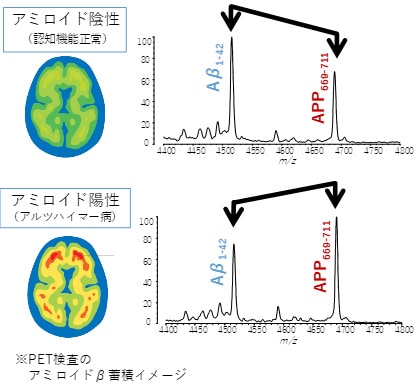
そして、共同研究を開始してから1年半後、アルツハイマー病の進行に伴って、新規発見ペプチドであるAPP669-711の量がAβ1-42よりも多くなる傾向があることを見出しました。つまり、“APP669-711/Aβ1-42”を新しいバイオマーカーとすることで、アルツハイマー病変(アミロイドβ蓄積)のある方とない方を高い精度で分離できる可能性が示唆されました。
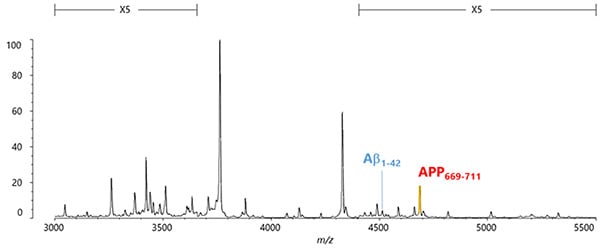
・ 特許番号:特許第06410810号
・ 論文:Proc Jpn Acad Ser B Phys Biol Sci. 2014;90(9):353-364.
アミロイドβの蓄積状態に応じて、Aβ1-42とAPP669-711の強度比が変わるのは、2つのペプチドの凝縮性の違いに起因すると考えられます。
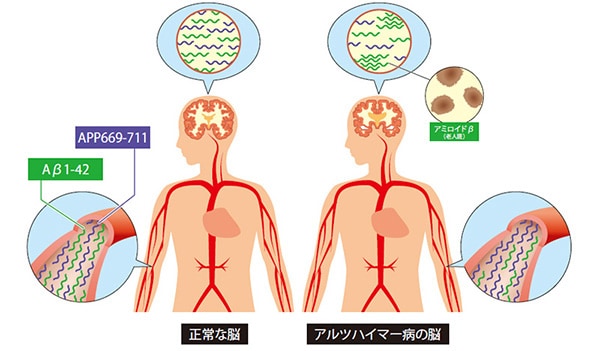
脳内で産生されたAβ1-42の一部は、健常者でも脳脊髄液や血液に漏出しています。
脳内でアミロイドβの蓄積が始まると、産生されたAβ1-42は次から次へとアミロイドβに結合(凝集)し、血液への漏出は減ります。一方、APP669-711は両端のアミノ酸配列に違いがあり、Aβ1-42と比較して大幅に自己凝集性が低くなります。したがって、アミロイドβに結合しにくく、脳内のアミロイドβ蓄積に関わらず一定の割合で血液に漏出していると考えられます。
また、Aβ1-42の漏出量は、アミロイドβ蓄積状態だけではなく個々人の全身状態に影響を受けて変動します。同じように影響を受けるAPP669-711の漏出量と比を取ることで、全身状態の影響を排除してアミロイドβ蓄積状態に起因する変動だけを取り出すことができます。
・ 論文:Nature (2018) doi:10.1038/nature25456
記載されている技術、製品等は研究用です。医薬品医療機器法に基づく体外診断用医薬品あるいは医療機器として承認・認証等を受けておりません。治療診断目的およびその手続き上での使用はできません。
共創
本技術は、島津製作所のMS分析技術と国立長寿医療研究センターの認知症研究知見の融合によって確立されました。
国立長寿医療研究センターWebページ


