Backnumber
Backnumber
大阪大学 畑澤順 教授
「起」と「結」の間にあるものは?

病気には必ず原因と、結果としての症状がある。
原因と結果を結びつけるのは比較的容易だが、その間、生体内でどう病気が進行しているのかについてはわからないことも多い。
その闇の可視化に挑む一人の医師に迫った。
医学部で初の大規模分子イメージング施設
大阪大学医学部は、昨夏、実験動物専用のPET分子イメージングセンターを設立した。医学部としては日本で初めてとなる施設だ。
分子イメージングとは、生きている体のなかで代謝活動などにより分子が発生したり消滅したりするプロセスを可視化する手法だ。この施設には、PETなどの核医学撮影装置のほか、体内の分子に結合して標識となる放射性トレーサーを製造するサイクロトロン装置もあり、世界最高レベルの装置群を揃えている。
「24時間、すべての装置を動物の病態観察に使える。これは画期的なことです。学内はもちろん、学外の研究機関や研究者にも開放しています」
同大大学院医学系研究科の畑澤順教授は、そう顔を輝かせる。
病気はいかにして病気となるのか
人のDNA解読がほぼ完了したのは2000年のことだった。その後、DNAの組み合わせからなる遺伝子の働きが次々と解明され、いまやある遺伝子の異常が、特定の病気の原因となるといった「原因と結果」の発見が、日常的に新聞紙上を彩るようになった。
だが、「遺伝子と症状の間にある距離は、あまりにも遠い」と畑澤教授は訴える。
「遺伝子のどこに異常があると、どういう症状が出るのかということはわかった。でも、それだけでは医師も製薬会社も何も手を出すことはできないのです。遺伝子の異常でどんなタンパク質の異常が生まれ、どんな代謝の異常が起こっているのか。病気がどこから始まってどう進行していくのか。こうした遺伝子と症状の間をつなぐ過程がわかって初めて、治療や創薬のターゲットが絞られてくるのです」
生体内での病気の進行を目で確認できる
生きている生体内部で何が起こっているかを画像として示す。これこそがPET分子イメージングに期待される役割だ。かつては病気の人の体の内部で何が起こっているかを確かめるためには、亡くなった後、解剖してみるしかなく、そこにはすでに病気が進行した末の組織があるだけで、「結果」を見ることしかできなかった。しかし、分子イメージングを用いれば、初期の段階でどこが損傷し、どのように機能障害が進行していくかといったことが、手に取るように見える。マウスなどの実験動物であれば、試験的な治療法を施した過程と結果を見ることができ、どのように機能が改善されるかなども観察できる。
「一大パラダイムシフトです。いままでは推理するしかなかった過程を、目で見て判断して、確実な現象に基づいて研究できる。PET分子イメージングは、医療・創薬研究の進展を加速化させるでしょう」(畑澤教授)
同センターでは、島津の実験動物用PETイメージング装置も稼働している。代表的な実験動物であるマウスの脳は小豆粒ほどしかないが、その機能をも克明に可視化する高い分解能を有し、教授らの研究を後押ししている。

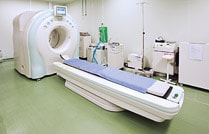
(上)併設する阪大病院で稼働している、島津のPET/CT「Eminence-G SOPHIA」
(下)PET分子イメージングセンターで稼働している島津の 中・大動物用PET装置
認知症のメカニズム解明に向けて
畑澤教授はPET装置の草創期から一貫してPETの研究に取り組んできた。PETを用いた脳循環代謝、脳機能の研究における第一人者でもある。
教授の追い続けているテーマの一つに認知症の研究がある。
たとえばアルツハイマー病。亡くなった方の脳を調べると、アミロイドというタンパク質が蓄積していることや、大脳皮質、海馬が萎縮していることは、以前からわかっていた。しかし、それは最終的な結果であって、認知症がどのように始まりどのように進行するかは、長く不明とされていた。
「90年代に、島津のPETのイメージング装置を使って観察したところ、アルツハイマー病の初期段階では、海馬や大脳皮質ではなく、後部帯状回という部分の機能が落ちていることがわかったんです。帯状回は自分は何者であるかというアイデンティティーを司っている部分で、通常、脳においてブドウ糖の代謝がもっとも活発なところです。ところがアルツハイマー病は、残酷にもこのアイデンティティー部分から壊していっていたのです。優れた分解能があったからこそ見つけられた成果です」
近年の研究で、脳についてさらに詳しいことがわかってきている。
「いま注目しているのは、神経細胞の働きをサポートしているグリア細胞。脳の神経細胞は150億ですが、グリア細胞は1500億個あります。アルツハイマー病ではなんらかの要因でこれが障害を受けているのですが、まだまったく手つかずなのです。グリア細胞の機能を解明できれば、この病気を克服するヒントが見つかるかもしれません」

大阪大学大学院医学系研究科
放射線統合医学講座(核医学) 教授 医学博士
畑澤 順 (はたざわ じゅん)
秋田県出身。1983年、東北大学大学院医学系研究科博士課程修了。東北大学サイクロトロンRIセンター、秋田県立脳血管研究センター勤務を経て、2002年、大阪大学大学院医学系研究科生体統合医学専攻生体情報医学講座教授。大阪大学医学部附属病院放射線部部長、同病院長補佐、同PET分子イメージンセンターセンター長。専攻はPETを用いた脳循環代謝および脳機能の研究、PET-MRI装置の開発。