掲載されている内容はすべて発表日当時のものです。その後予告なしに変更されることがありますのであらかじめご了承ください。
2020年7月29日 | プレスリリース
新たな化学構造解析技術が拓く、新たな天然物骨格構造の発見
~新規質量分析技術により、有用天然物の新たな一大グループが発見された~
発表のポイント
- 新しい医薬品のリード化合物として期待できる、脂肪酸とペプチド化合物がハイブリッド化した特徴的な天然物骨格の新たなグループ・PK/RiPPハイブリッドリポペプチドを発見しました。
- 非常に長い繰り返し構造を持つ複雑な炭素鎖化学構造を効率的に解析する新たな気相ラジカル照射を用いた質量分析法(HiRID™-MS / MS)を開発、適用することにより、初めて化学構造が解明できました。詳しくはこちら(島津製作所田中耕一記念質量分析研究所ページへのリンク)
- 新たな解析手法の確立と、それによる新たな天然物グループの発見により、天然物の構造多様性が広がり、天然物の医薬品としての利活用がより一層広がることが期待できます。
発表概要
東京大学大学院農学生命科学研究科 尾仲宏康特任教授、大学院薬学系研究科 阿部郁朗教授、島津製作所田中耕一記念質量分析研究所 田中耕一所長らのグループは、新しい医薬品の原料として期待できる、脂肪酸とペプチド化合物がハイブリッド化した特徴的な天然物骨格を有するPK/RiPPハイブリッドリポペプチド(注1)を発見しました(図1)。PK/RiPPハイブリッドリポペプチド化合物群は従来の分析法では化学構造の決定が困難でありましたが、今回新たに島津製作所田中耕一記念質量分析研究所によって開発された、ラジカル原子/分子を照射することでC–C結合切断フラグメントを生成するHiRID-MS / MS装置(注2)によって決定されました(図2)。
今回発見された化合物はグラム陽性細菌の増殖を阻害するゴードビオニン(goadvionin)と命名したPK/RiPPハイブリッドリポペプチドです(図3)。32個の炭素からなる非常に長い鎖長の脂肪酸(注3)と8個のアミノ酸からなるペプチド化合物(注4)がハイブリッド化した複雑な化学構造であり、既存の解析手法では化学構造の決定は困難でした。ゴードビオニンの生合成に必要な遺伝子を解析し、生合成の過程を解明した結果、ゴードビオニンと構造が類似したPK/RiPPハイブリッド化合物は微生物に広く分布していることが明らかになりました(図4)。
今回の結果は、新たな化学構造解析技術により、有用天然物の新たな一大グループが発見されたことを示しており、化合物分析技術開発と天然物探索研究の連携により、天然物の医薬品等へ応用が広がることを示した成果です。
発表内容
微生物などが生産する天然物は医薬品にも利用される重要な化学物質です。人類はこれまでの長い歴史の中でペスト、結核などさまざまな感染症に悩まされてきていました。それに対して人類は、青カビの生産する抗生物質であるペニシリンの発見以降、結核の特効薬ストレプトマイシンなど、さまざまな天然物由来抗生物質を開発し、感染症を制圧してきました。しかしながら、現時点でもコロナウイルスを始め、新たな感染症が続々と発生しており、それに対する薬剤の開発が急務となっています。薬剤開発において重要な点の一つは新たな薬剤となり得る候補化合物を多数取りそろえることですが、天然物に頼る現状では候補化合物の種類に限界があります(注5)。一方、化学合成法を用いて複雑な構造の化合物を多数合成することも行われていますが、構造が複雑になればなるほどコストと時間がかかり、天然物のような複雑な化学構造を容易に作ることが難しいという問題があるため、新たな天然物の発見は医薬品開発における重要な研究テーマの一つであります。
今回、東京大学大学院農学生命科学研究科 尾仲宏康特任教授、大学院薬学系研究科 阿部郁朗教授、島津製作所田中耕一記念質量分析研究所 田中耕一所長らのグループは、PK/RiPPハイブリッドリポペプチドと呼ばれる天然物の新たな一群がさまざまな微生物種に存在することを明らかにしました。
脂肪酸とペプチドがハイブリッド(融合)化した化学構造は、両化合物のさまざまな組み合わせが可能となるため、天然物の化学構造と生理活性の多様性を拡げることにつながります。これまでに脂肪酸とペプチドが融合した化合物(リポペプチド)の一部は医薬品として発売されています。研究グループは、従来のリポペプチドとは微生物内での合成の過程が異なり、化合物の構造もリポペプチドとは大きく異なる一群の化合物群・PK/RiPPハイブリッドリポペプチドが天然に存在していることを示しました。
今回、ゴードビオニン(goadvionin)と命名したグラム陽性菌の増殖を阻害するPK/RiPPハイブリッドリポペプチドが放線菌Streptomyces sp. TP-A0584(注6)より発見されました。ゴードビオニンは、極端に長いアシル鎖(トリメチルアミノ32炭素アシル鎖、注7)と、複雑な修飾を受けたペプチド構造(アビオニン含有ランチペプチド、注8)で構成されています(図1)。極端に長いアシル鎖の6つのヒドロキシ基と1つの二重結合の位置は、従来の分析技術では構造解析が困難であったため、今回新たに島津製作所田中耕一記念質量分析研究所によって開発された、ラジカル原子/分子を照射することでC–C結合切断フラグメントを生成するHiRID-MS / MS装置によって決定されました(図2)。
ゴードビオニンの生合成遺伝子を解析し、その生合成の過程を明らかにしたところ、アシル鎖とペプチド鎖が結合してハイブリッド化する反応は、GNATスーパーファミリーに属するアシルトランスフェラーゼ(注9)・GdvGが触媒することが明らかとなりました。この反応は従来のアシルトランスフェラーゼとは異なり、アシルキャリアプロテイン(ACP)につながれた非常に長いアシル鎖をペプチド部分のN末端アミノ基に転移する反応であることが明らかとなりました(図3)。この特徴的なgdvG遺伝子を指標にして、これまでに報告されている微生物ゲノムを探索したところ、放線菌を中心にさまざまな微生物がgdvG相同遺伝子を有していることが明らかとなりました(図4)。
本研究により、(1)幅広い微生物種がPK/RiPPハイブリッドリポペプチドを生産していること、(2)アシル鎖とペプチドのハイブリッド化をGdvG様アシルトランスフェラーゼが触媒することがPK/RiPPハイブリッドリポペプチドの生合成における一般的な戦略であること、が示されました。また、今回の成果のように、新しい化学構造解析技術を天然物探索研究と組み合わせることで、従来発見できなかった新たな天然物群が今後も効率的に発見できることが期待できます。
本成果はNature ChemistryにAcyltransferase that catalyses the condensation of polyketide and peptide moieties of goadvionin hybrid lipopeptidesのタイトルで掲載されました。
なお、本研究を行った東京大学大学院農学生命科学研究科微生物潜在酵素寄付講座は、天野エンザイム株式会社の寄付によって設立された寄付講座です。
田中耕一記念質量分析研究所は、2002年にノーベル化学賞を受賞した田中耕一博士(現・所長)が、質量分析装置の新規技術と応用技術の開発を推進するため、2003年1月に株式会社島津製作所内に開所した研究所です。
発表雑誌
| 雑誌名 | : | 「Nature Chemistry」(7月27日オンライン版) |
| 論文タイトル | : | Acyltransferase that catalyses the condensation of polyketide and peptide moieties of goadvionin hybrid lipopeptides |
| 著者 | : | Ryosuke Kozakai, Takuto Ono, Shotaro Hoshino, Hidenori Takahashi, Yohei Katsuyama, Yoshinori Sugai, Taro Ozaki, Kazuya Teramoto, Kanae Teramoto, Koichi Tanaka, Ikuro Abe, Shumpei Asamizu, and Hiroyasu Onaka |
| DOI番号 | : | 10.1038/s41557-020-0508-2 |
| アブストラクト URL |
: | https://www.nature.com/articles/s41557-020-0508-2 |
用語解説
(注1)PK/RiPPハイブリッドリポペプチド:PKはポリケタイド化合物の略で、ポリケトン鎖が修飾を受けた構造で、天然物の主要な炭素骨格構造の一つです。RiPPはリボソーム翻訳系翻訳後修飾ペプチドの略で、ペプチド化合物(注4)が翻訳後修飾を受けた構造をしており、やはり、天然物の主要な炭素骨格構造の一つです。PK/RiPPハイブリッドリポペプチドはPKとRiPPsがハイブリッド(縮合)化した構造をしています。
(注2)気相ラジカル照射を用いた質量分析法(HiRID-MS / MS, Highly-integrated Radical Induced Dissociation-MS/MS):質量分析計(MS)において測定サンプルイオンにラジカル原子/分子を照射することにより、従来手法では断片化が難しかったC-C結合の断片化を可能にした質量分析法。 ※特許第06229790号と他3件
(注3)脂肪酸:脂肪酸は長い炭素鎖(アシル鎖)を有するカルボン酸(R-COOH)の総称です。例えば、植物油に含まれているオレイン酸やリノール酸は炭素鎖長が18の脂肪酸です。本研究で発見されたゴードビオニンは炭素鎖長31(炭素数32)の非常に長い脂肪酸が含まれています。
(注4)ペプチド化合物:複数のアミノ酸がペプチド結合(-CO-NH2-)で連結された化合物の総称。ゴードビオニンにおいては8個のアミノ酸が連結したペプチド構造を有します。タンパク質も広義のペプチド化合物ですが、連結されるアミノ酸の数が多く、数百から数千個連結されています。
(注5)天然物に頼る現状では種類の限界がある:これまで人類は微生物、植物等さまざまな生物から医薬品の原料となる天然物の探索を行なってきました。その結果、近年では、新規構造の天然物の発見数が減少しており、主要な天然物は既に取り尽くされたともいわれています。現在では稀少な天然物を発見するために、特殊な環境に生息する稀少な微生物の探索やゲノム情報を活用した効率的な探索法も行われていますが、必ずしも新規天然物を効果的に発見できているわけではないのが現状です。
(注6)放線菌:放射状に菌糸を生やして生育する真性細菌の一群で多様な種を有します。主に土壌中に広く生息し、環境中では有機物の分解者としての役目を果たしています。産業的には抗生物質をはじめ、医薬品の原料となる多様な二次代謝産物を作る菌として知られており、結核の特効薬ストレプトマイシンや抗生物質エリスロマイシン、免疫抑制剤タクロリムス、抗寄生虫薬エバーメクチンなどを生産します。
(注7)極端に長いアシル鎖(トリメチルアミノ32炭素アシル鎖):アシル鎖は炭素が連続して連結し、かつその分子の片側末端がCOである構造、つまりカルボン酸からOHを除いた構造(R-CO-)を示します。ゴードビオニンの場合はRの構造が極端に長く、31個の炭素が連続して連結された構造を有しており、分岐メチル基を含めて32個の炭素原子から成っており、さらにその末端はトリメチルアミン(CH3)3N-になっています。
(注8)複雑な修飾を受けたペプチド構造(アビオニン含有ランチペプチド):ゴードビオニンのペプチド部分はリボゾームによって翻訳合成された後に、GdvKC, GdvDの二つの酵素によってアビオニン構造へと翻訳後修飾されます。
(注9)GNATスーパーファミリーに属するアシルトランスフェラーゼ:アシルトランスフェラーゼとはアシル基を転移する触媒反応を有する酵素です。一般的にはCoAに結合したアシル基(アシルCoA)をアミノ基に転移する反応を触媒します。しかし、GdvGの基質はCoA 体ではなく、アシルキャリアプロテイン(ACP)に結合したアシル基を基質にして転移反応を行う点がユニークです。
添付資料
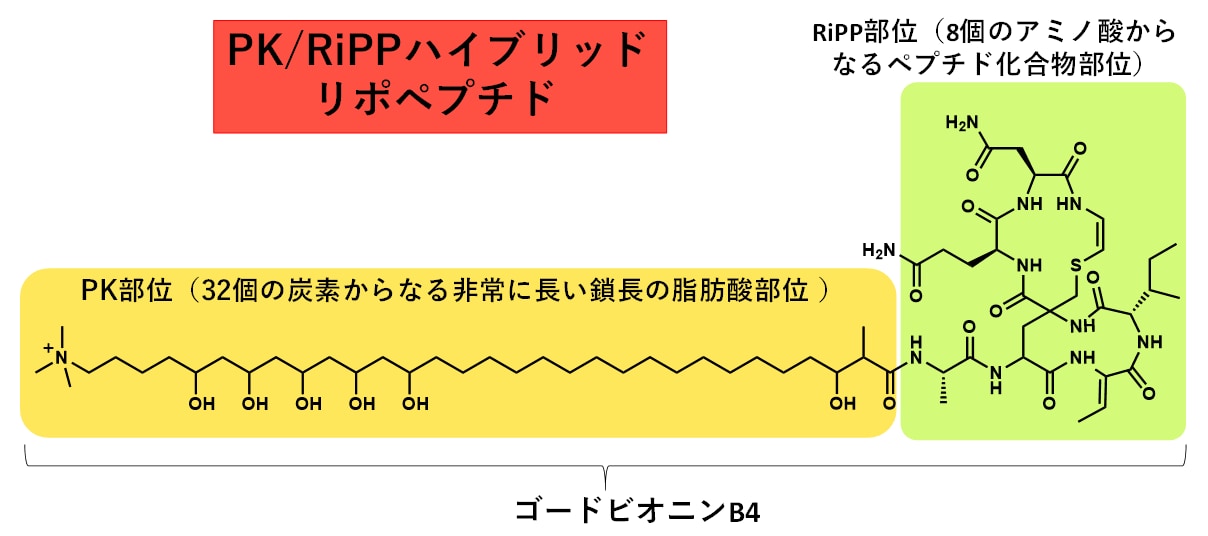
図1 PK/RiPPハイブリッドリポペプチドの一種、ゴードビオニンの化学構造
今回8種類発見されたゴードビオニン群のうち、ゴードビオニンB4の化学構造です。PK部位とRiPP部位の二つの構造がハイブリッド化しており、他に類を見ない非常に長い直鎖脂肪酸を有しているのが特徴です。
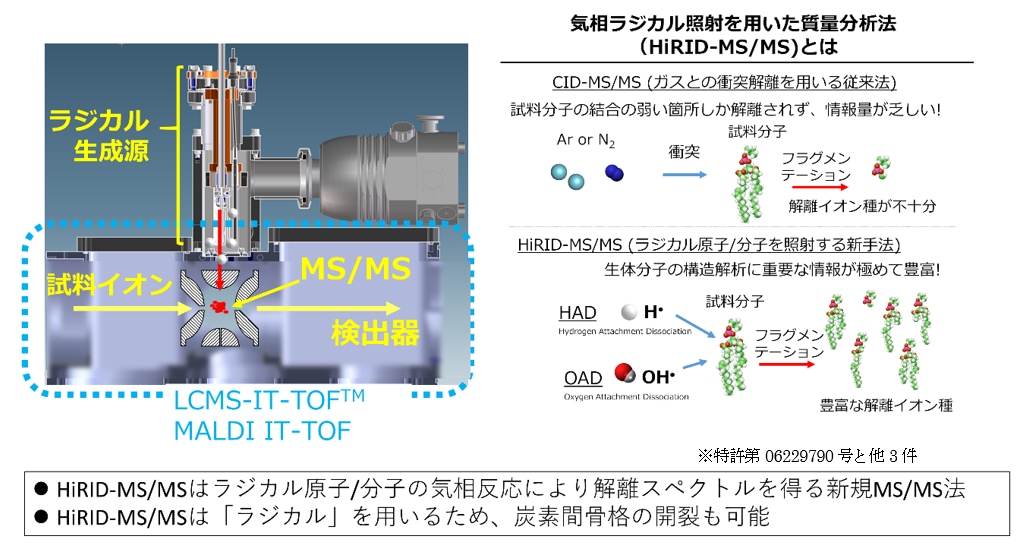
図2 気相ラジカル照射を用いた質量分析法(HiRID-MS / MS)の概略
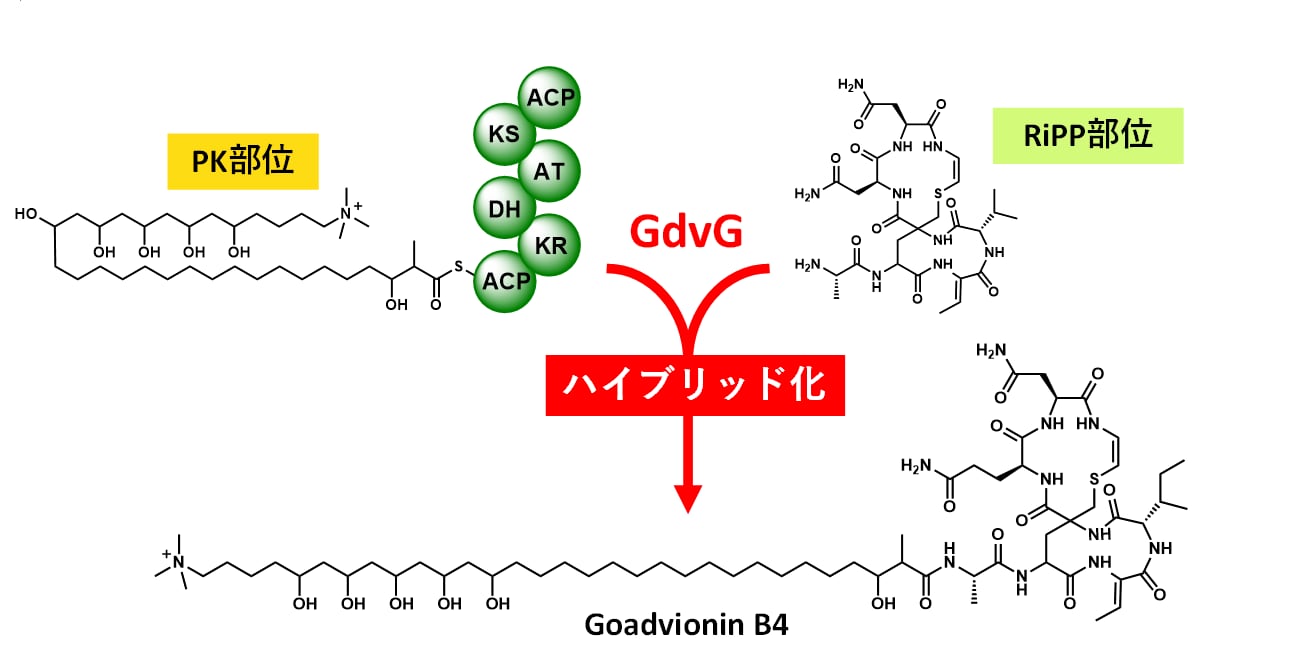
図3 ゴードビオニン生合成過程におけるハイブリッド化機構
ACPにロードされたPK部位がGdvGアシルトランスフェラーゼ酵素によってRiPP部位のアミノ末端とハイブリッド化することによりゴードビオニンが生合成されます。
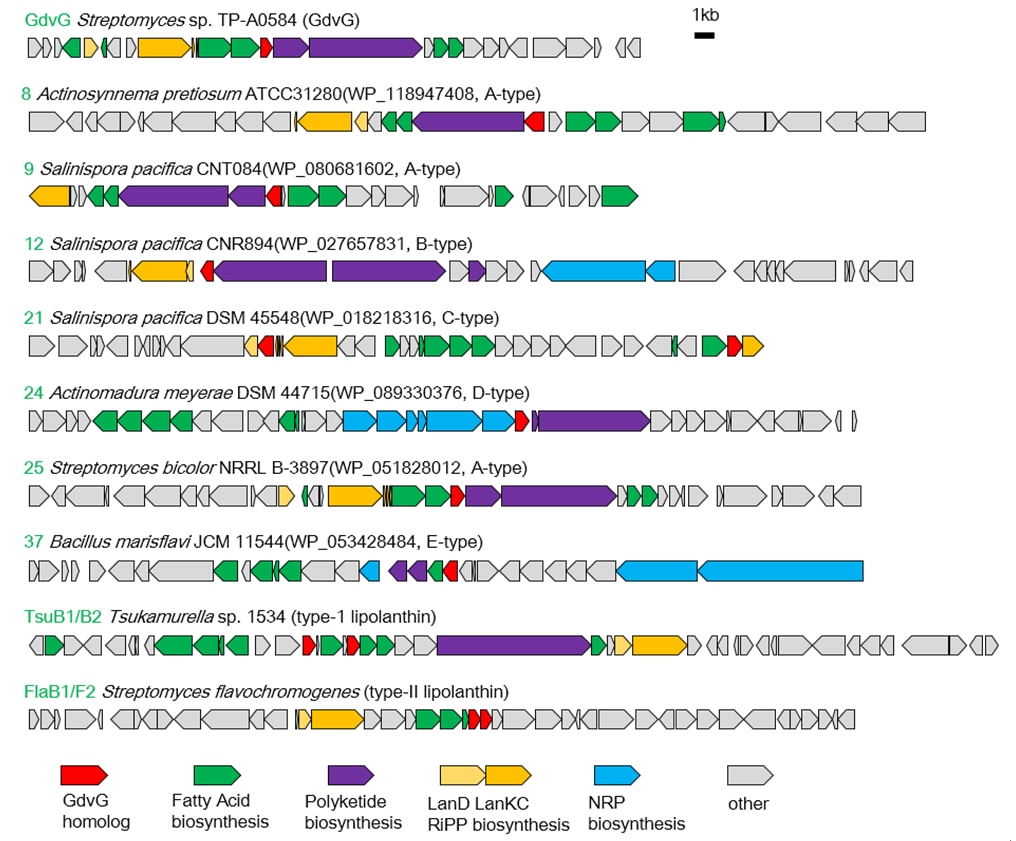
図4 gdvG相同遺伝子は幅広い微生物種内ゲノムに存在している。
gdvG相同遺伝子が発見された微生物ゲノムの遺伝子配置の様子を示しています。一番上の遺伝子マップは今回発見されたゴードビオニン生合成遺伝子群です。以下、さまざまな微生物種にgdvG相同遺伝子が存在していることが明らかになりました。gdvG相同遺伝子は赤で示しています。
※HiRIDおよびLCMS-IT-TOFは、株式会社島津製作所の商標です。


