- HOME
- > Ampdirect™ 2019-nCoV検出キット
遺伝子増幅法(1step RT-PCR)により,新型コロナウイルス(SARS-CoV-2)のRNAを検出するキットです。生体試料(鼻咽頭拭い液,唾液を推奨)からRNA精製することなく簡単な前処理だけで使用できます。
体外診断用医薬品
製造販売承認番号 30200EZX00065000
 試料からのRNA精製は不要,このキットだけで検出できます。
試料からのRNA精製は不要,このキットだけで検出できます。 前処理(加熱),反応/検出で約70分※1です。
前処理(加熱),反応/検出で約70分※1です。- Ampdirect Technology技術を応用し,新型コロナウイルスのPCR検出時間を短縮(特許出願中)
※1 リアルタイムPCR装置によって反応時間は前後します。同時に取扱う検体数が多くなるにつれ,試料や試薬調製の時間が増加します。
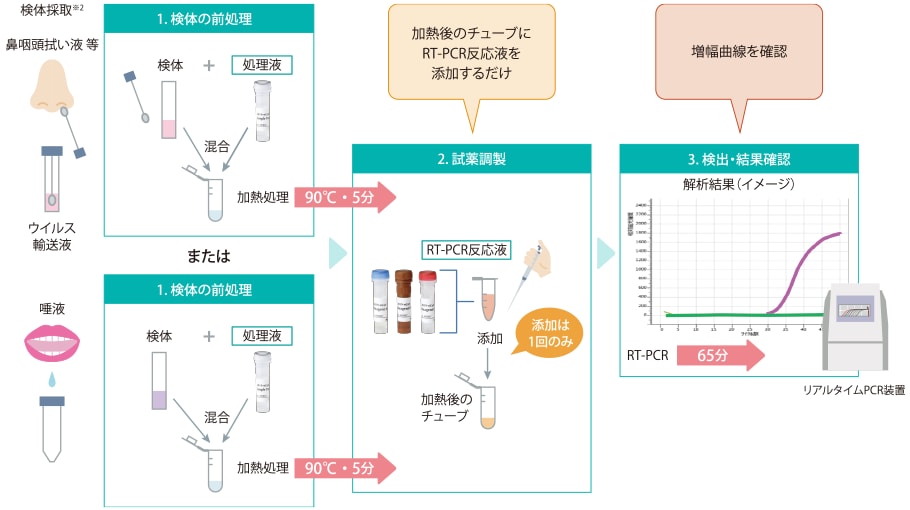
※2 検体採取,取扱いについては必要なバイオハザード対策をとってください。
各種臨床検体の取扱い,検体輸送については,厚生労働省より公表されている「新型コロナウイルス感染症 (COVID-19)病原体検査の指針」や,国立感染症研究所より公表されている「2019-nCoV (新型コロナウイルス)感染を疑う患者の検体採取・輸送マニュアル」を参照いただくよう,お願いいたします。
製品情報
| 品 名 | P/N | 備 考 |
|---|---|---|
| Ampdirect™ 2019-nCoV 検出キット |
227-20000-21 | 検出対象:新型コロナウイルス(SARS-CoV-2)のN(Nucleocapsid)遺伝子領域2か所(CDC N1,N2) |
| 検出原理:1step RT-PCR/加水分解プローブ検出法 | ||
| 包装単位:100テスト | ||
| 貯蔵方法:-35℃~ -15℃ | ||
| 有効期間:12ヶ月(使用期限は外装に記載しています) |
- 注意)
- ・本品の判定が陰性であっても,SARS-CoV-2感染を否定するものではありません。
- ・新たに出現した変異株は検出ができないことがあります。
- ・検体中のウイルス量や夾雑物の多寡などによって検出できない場合があります。
関連文書(ダウンロード可能)
製品構成
| 項 目 | 数 量 | 容 量 |
|---|---|---|
| ① 処理液(2019-nCoV Sample Treatment Reagent) | 1本 | 500 µL |
| ② 反応液A(2019-nCoV Reagent A) | 1本 | 650 µL |
| ③ 反応液B(2019-nCoV Reagent B) | 1本 | 650 µL |
| ④ 反応液C(2019-nCoV Reagent C) | 1本 | 200 µL |
オプション
| 項 目 | 備 考 |
|---|---|
| 陽性コントロール スタンダードRNA for nCoV | ※ 本製品は本試薬キットの陽性コントロールRNA溶液です。 |
RNA精製を不要にするAmpdirect Technology
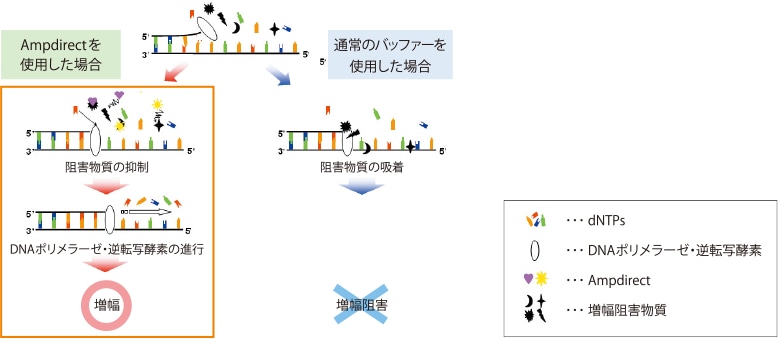
生体試料に含まれる正電荷物質(ある種のタンパク質等)は鋳型(DNA/RNA)に,負電荷物質(ある種の糖,色素等)はポリメラーゼ(DNA)に吸着し,PCRを阻害すると考えられます。Ampdirectにはこれらの物質を抑制する働きがあるので,生体試料から直接RT-PCRが可能になります。
※キットご使用の際には添付文書をよくお読みください。
※診断は厚生労働省より発表されている医療機関・検査機関向けの最新情報を参照し,本品による検査結果のみで行わず,臨床症状も含めて総合的に判断してください。
Ampdirectは,株式会社島津製作所の商標です。
本文書に記載されている会社名,製品名,サービスマークおよびロゴは,各社の商標および登録商標です。
なお,本文中では「TM」,「®」を明記していない場合があります。
外観および仕様は,改良のため予告なく変更することがありますのでご了承ください。
製造販売元
株式会社島津製作所 〒604 -8511 京都市中京区西ノ京桑原町1
>> お問い合わせ